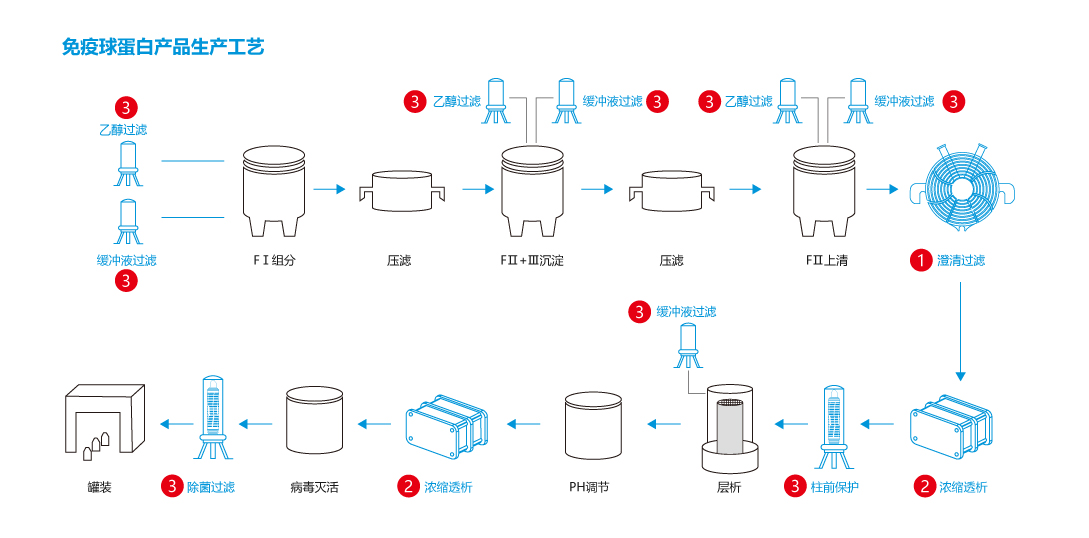
血液制品属于生物制品范围,主要指以健康人或特异免疫人血浆为原料,采用生物学工艺或分离纯化技术制备的生物活性制剂,包括各种人血浆蛋白制品,包括人血白蛋白、人胎盘血白蛋白、静脉注射用人免疫球蛋白、各类免疫球蛋白(乙型肝炎、狂犬病、破伤风免疫球蛋白)、人凝血因子Ⅷ、人凝血酶原复合物等。赛普能够为血液制品生产中的澄清过滤、超滤、除病毒过滤和终端除菌过滤提供全面解决方案。

① 澄清:
澄清步骤主要目的是清除在细胞收获液里的细胞和颗粒杂质,传统工艺通过二级离心去除杂质。目前深层过滤开始普遍应用在澄清工艺步骤。深层过滤指的是利用多孔介质从流动相中截留固体颗粒而不是表面截留,且一般介质表面都带有正电荷,可以通过静电吸附的方式来拦截杂质颗粒。
适用产品:SaiClear® P系列及S系列澄清过滤器 了解详情→
② 超滤:
此步超滤目的主要是把样品浓缩后换液到制剂缓冲液里。此步骤除常规通量外,需要关注目标蛋白的耐剪切力。
适用产品: TanFlux®Ⅱ PES 超滤膜包 了解详情→
③ 除病毒过滤:
除病毒过滤是生物制药抗体领域常用的病毒去除方法。其利用孔径大小排除原理,将病毒截留于过滤膜表面。除病毒过滤膜孔径为20 nm。低pH病毒灭活法主要灭活脂包膜病毒,而非脂包膜病毒的清除,如小白鼠病毒(MMV),因其对化学失活具有很高的抵抗力,因此需要除病毒滤膜来去除。
适用产品:Valpha®除病毒过滤器 了解详情→
④ 除菌过滤:
除菌过滤是指从液体流中去除微生物而对产品本身质量没有负面影响的工艺过程。除菌过滤利用物理阻留的方法将液体或空气钟的细菌除去,以达到无菌目的。除菌过滤器的等级一直存在着争议,主要原因是各生产商在测量孔径方面缺乏一致性。由于根据孔径来划分除菌级过滤器的定义方法具有其局限性,所以法规上是根据细菌截留能力来定义过滤器的等级。PDA TR26 指出:在规定的条件下,在有效的过滤器表面积内每平方厘米截留B. diminuta ATCC 19146的能力达到10⁷的过滤器定义为除菌级过滤器。
适用产品:终端料液除菌过滤:SaiPress® 0.22μm 了解详情→
培养基过滤:SaiPress® 0.45+0.22μm 了解详情→
缓冲液过滤及柱前保护:PolySai 预过滤器了解详情→、
SaiPress® 0.22μm 了解详情→
气体过滤及呼吸器:Filgiant® 0.22μm 了解详情→